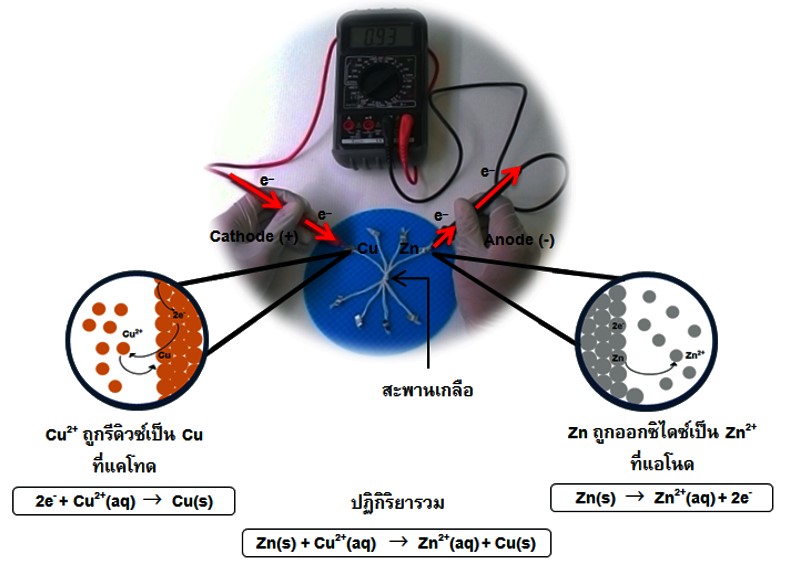
การสร้างเซลล์กัลวานิกอย่างง่ายที่ทำจากเส้นด้ายเพื่อศึกษาไฟฟ้าเคมี
Main Article Content
Abstract
Malai Sawangpop, Purim Jarujamrus, Maliwan Amatatongchai, Suparb Tamuang and Sanoe Chairam
รับบทความ: 17 มีนาคม 2560; ยอมรับตีพิมพ์: 10 ตุลาคม 2560
บทคัดย่อ
วัตถุประสงค์หลักของบทความวิจัยนี้คือสร้างชุดการทดลองเซลล์กัลวานิกอย่างง่ายที่ทำจากเส้นด้าย ชุดอุปกรณ์นี้ประกอบด้วยแผ่นโลหะ (ทองแดง เงิน สังกะสี ตะกั่ว ดีบุก เหล็ก อะลูมิเนียม และแมกนีเซียม) สารละลายโลหะและสารละลายโพแทสเซียมไนเตรตทำหน้าที่เป็นขั้วไฟฟ้า ไอออนของโลหะ และอิเล็กโทรไลต์ ตามลำดับ ในบทความงานวิจัยนี้ นอกจากเส้นด้ายทำหน้าที่เป็นตัวรองรับปฏิกิริยาระหว่างแต่ละครึ่งเซลล์แล้ว ยังทำหน้าที่เป็นสะพานเกลือสำหรับอิเล็กโทรไลต์ด้วย ผลการทดลองแสดงให้เห็นว่า ความต่างศักย์ไฟฟ้าที่วัดได้ให้ผลที่ไม่แตกต่างกับทฤษฎีที่คำนวณจากสมการของเนินสท์ ชุดอุปกรณ์นี้ยังสามารถศึกษาผลของความเข้มข้นที่มีต่อแรงเคลื่อนทางไฟฟ้าได้อีกด้วย ชุดอุปกรณ์นี้สามารถนำไปประยุกต์เป็นสื่อการสอนเคมีไฟฟ้าสำหรับนักเรียนในระดับมัธยมศึกษาเนื่องจากง่ายต่อการสร้างเซลล์กัลวานิก
คำสำคัญ: เซลล์กัลวานิก เส้นด้าย ไฟฟ้าเคมี ชั้นมัธยมศึกษา
Abstract
The main purpose of this research article was to fabricate simple galvanic cells using cotton thread. This device contains various metal strips (Cu, Ag, Zn, Pb, Sn, Fe, Al and Mg), metal solutions, and potassium nitrate solution serving as electrodes, metal ions, and electrolyte, respectively. In this article, cotton thread is not only used to be a support for reactions between each half-cell, but also a salt bridge for electrolyte. The results showed that the observed cell potentials, (Obsd) were slightly different from the theoretical cell potentials, (Theor), calculated from the Nernst equation. This device also can be used to investigate the effect of concentrations on the electromotive force (emf). This device can be applied as a teaching tool of electrochemistry for students at the secondary school level because of an easy way to fabricate galvanic cells.
Keywords: Galvanic cell, Cotton thread, Electrochemistry, Secondary school
Downloads
Article Details

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
References
Brosmer, J. L., and Peters, D. G. (2012). Gal-vanic cells and the determination of equilibrium content. Journal of Chemical Education 89(6): 763–766.
Chang, R. (2012). Chemistry. 10th ed. Bangkok: McGraw-Hill.
Chatmontree, A., Chairam, S., Supasorn, S., Amatatongchai, M., Jarujamrus, P., Tamuang, S., and Somsook, E. (2015). Student fabrication and use of simple, low-cost, paper-based galvanic cells to investigate electrochemistry. Journal of Chemical Education 92(6): 1044–1048.
Eggen, P. O., and Skaugrud, B. (2015). An easy to-assemble three-part galvanic cell. Journal of Chemical Education 92(6): 1053–1055.
Khattiyavong, P., Jarujamrus, P., Supasorn, S., and Kulsing, C. (2014). The development of small scale and low-cost galvanic cells as a teaching tool for electrochemistry. Journal of Research Unit on Science, Technology and Environment for Learning 5(2): 146–154.
Suwannapruek, R. (2014). General Chemistry 2. Bangkok: Witayaphat. (in Thai)
Whitten, K. W., Davis, R. E., Peck, L. M., and Stanley, G. G. (2007). Chemistry. 8th ed. Belmont, USA: Thomson Brooks/Cole.