การสังเคราะห์ฟลูออเรสเซนต์เซ็นเซอร์ชนิดใหม่ประเภท Schiff base สำหรับการวิเคราะห์คอปเปอร์ (II) ไอออน
Main Article Content
Abstract
Pran Aussawaponpaisan, Phoomirut Nusuwan, Pan Tongraung, Mayuso Kuno, Kem Pumsa-ard and Piyada Jittangprasert
รับบทความ: 11 ธันวาคม 2560; แก้ไขบทความ: 21 พฤษภาคม 2561; ยอมรับตีพิมพ์: 31 กรกฎาคม 2561
บทคัดย่อ
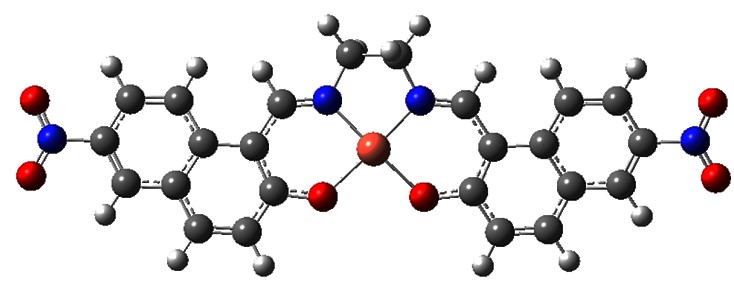
เซ็นเซอร์ทางเคมีชนิดใหม่ 1,1'–((1E,1'E)–(ethane–1,2–diylbis(azanylylidene))bis (methanylylidene))bis(6–nitronaphthalen–2–ol) (L) ได้รับการออกแบบและสังเคราะห์ขึ้นจากปฏิกิริยาคู่ควบระหว่าง ethylenediamine กับ 2–hydroxy–6–nitro–1–naphthadehyde โมเลกุลประกอบด้วยหมู่ Schiff base และหมู่ hydroxyl ทำหน้าที่เป็นหน่วยจับไอออนของโลหะ และหมู่ 2–hydroxy–6–nitronapthalene เป็นหน่วยให้สัญญาณการวาวแสง เมื่อศึกษาความจำเพาะเจาะจงกับไอออนของโลหะหนักชนิดต่าง ๆ (Mn2+ Fe2+ Co2+ Ni2+ Cu2+ Zn2+ และ Cd2+) ด้วยเทคนิคฟลูออเรสเซนต์สเปกโทร-สโกปี พบว่า L เลือกจับจำเพาะเจาะจงกับ Cu2+ โดยเกิดการระงับการวาวแสงที่ความยาวคลื่น 540 นาโนเมตร อัตราส่วนการเกิดสารประกอบเชิงซ้อนระหว่างโมเลกุล L กับ Cu2+ เป็นแบบ 1:1 โดยมีค่าคงที่การระงับการวาวแสง (Ksv) ที่คำนวณจากข้อมูลการไทเทรตด้วยเทคนิคฟลูออเรสเซนต์สเปกโทรสโกปีเท่ากับ 1.65 x 105 M-1 นอกจากนี้ผลการศึกษาอันตรกิริยาที่เกิดขึ้นระหว่างลิแกนด์ L กับ Cu2+ ด้วยเทคนิคเคมีคอมพิวเตอร์โดยใช้ระเบียบวิธีการคำนวณ B3LYP/6–311G(d,p) พบว่า ผลการคำนวณที่ได้มีความสอดคล้องกับผลการทดลองเป็นอย่างดี เมื่อนำเซ็นเซอร์ L มาประยุกต์ใช้ในการวิเคราะห์ปริมาณ Cu2+ ในตัวอย่างน้ำผิวดิน พบว่า ในตัวอย่างมีปริมาณ Cu2+ อยู่ในช่วงความเข้มข้น 0.66±0.01 ถึง 0.87±0.11 มิลลิกรัมต่อลิตร โดยวิธีวิเคราะห์ที่พัฒนาขึ้นนี้มีช่วงความเป็นเส้น ตรง 2 ช่วง คือ 0.25–1.0 และ 1.5–25 มิลลิกรัมต่อลิตร และมีค่าขีดจำกัดต่ำสุดที่ตรวจวัดได้เท่ากับ 0.15 มิลลิกรัมต่อลิตร
คำสำคัญ: เซ็นเซอร์ทางเคมี ฟลูออเรสเซนต์ ชิฟเบส คอปเปอร์ (II) ไอออน ตัวอย่างน้ำ
Abstract
A novel chemosensor 1,1'–((1E,1'E)–(ethane–1,2–diylbis(azanylylidene))bis(methanylylidene))bis(6–nitronaphthalen–2–ol), (L) was designed and synthesized by coupling reaction between ethylenediamine and 2–hydroxy–6–nitro–1–naphthadehyde. The molecule composed of a Schiff base and a hydroxyl groups as a binding unit and a 2–hydroxy–6–nitronapthalene group as a fluorescence signaling unit. The selectivity studies between L and various metal ions (Mn2+, Fe2+, Co2+, Ni2+, Cu2+, Zn2+ and Cd2+) were carried out by fluorescence spectroscopy. The results indicated that L showed high selectivity for Cu2+ with significant fluorescence quenching at 540 nm. The stoichiometry of the complex between L and Cu2+ was 1:1 and the quenching constant (Ksv) of complex was calculated to be 1.65 x 105 M-1 using the fluorescence spectroscopy titration data. Furthermore, the interaction between ligand L and Cu2+ was evaluated by computational chemistry using a B3LYP/6–311G(d,p) level of calculation. The results showed that a good relatively agreement with the fluorescence spectroscopy experiments. Sensor L was successfully applied for the determination of Cu2+ in surface water samples. The results showed that the amount of Cu2+ were in range of 0.66±0.01 to 0.87±0.11 mg/L. In addition, the two linear calibration curves were obtained over the concentration range of 0.25–1.5 and 1.0–25 mg/L and the limit of detection (LOD) was at 0.15 mg/L.
Keywords: Chemosensor, Fluorescence, Schiff base, Copper (II) ion, Water sample
Downloads
Article Details

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
References
Chawla, H. M., Goel, P., and Munjal, P. (2015). A new metallo–supramolecular sensor for recognition of sulfide ions. Tetrahedron Letters 56: 682–685.
Dalapati, S., Jana, S., Alam, M.A., and Guchhait, N. (2011). Multifunctional fluorescent probe selective for Cu(II) and Fe(III) with dual–mode of binding approach. Sensors and Actuators B. 106: 1106–1111.
Dong, Y., Koken, B., Ma, X., Wang, L., Cheng, Y., and Zhu, C. (2011). Polymer–based fluorescent sensor incorporating 2,2–bipyridyl and benzo[2,1,3]thiadiazole moieties for Cu2+ detection. Inorganic Chemistry Communications 14: 1719–1722.
Ekmekci, Z. (2015). Highly selective fluorescence ‘turn-off’ sensors for Cu2+ in aqueous environments. Tetrahedron Letters 56: 1878–1881.
Ganguly, A., Ghosh, S., Kar, S., and Guchhait, N. (2015). Selective fluorescence sensing of Cu(II) and Zn(II) using a simple schiff base ligand: Naked eye detection and elucidation of photo induced electron transfer (PET) mechanism. SpectrochimicaActa Part A: Molecular and Biomolecular Spectroscopy 143: 72–80.
Hoffmann, S.K., Goslar, J., Lijewski, S, Tadyszak, K., Zalewska, A., Jankowska, A., Florczak, P., and Kowalak, S. (2014). EPR and UV–vis study on solutions of Cu(II) complexes and the complexes entrapped in zeolite A and ZIF–Cu(IM)2 Microporous and Mesoporous Materials 186: 57–64.
Huang, J., Xu, Y., and Qian, X. (2009). A col-orimetric sensor for Cu2+ in aqueous solution based on metal ion–induced deprotonation:deprotonation/protonation mediated by Cu2+–ligand interactions. Dalton Transactions 10: 1761–1766.
Jiang, J., Gou, C., Luo, J., Yi, C., and Liu, X. (2012). A novel highly selective colorimetric sensor for Ni(II) ion using coumarin derivatives. Inorganic chemistry Communications 15: 12–15.
Joseph, R., Ramanujam, B., Acharya, A., and Rao, C. P. (2009). Fluorescence switch–on sensor for Cu2+ by an amide linked lower rim1,3–bis(2–picolyl)amine derivative of calix[4]arene in aqueous methanol. Tetrahedron Letters 50: 2735–2739.
Khan, B., Shah, M.R., Ahmeda, D., Rabnawaz, M., Anis, I., Afridi, S., Makhmoor, T., and Tahir, M.N. (2016). Synthesis, characterrization and Cu2+triggered selective fluorescence quenching of Bis–calix[4]arene tetratriazolemacrocycle. Journal of Hazardous Materials 309: 97–106.
Li, W., Simmons, P., Shrader, D., Herrman, T. J., and Dai, S.Y. (2013). Microwave plasma–atomic emission spectroscopy as a tool for the determination of copper, iron, manganese and zinc in animal feed and fertilizer. Talanta 112: 43–48.
Liu, J., and Lu, Y. (2007). A DNA enzyme catalytic beacon sensor for paramagnetic Cu2+ ion in aqueous solution with high sensitivity and selectivity. Journal of American Chemical Society 129: 9838–9839.
Mashhadizadeha, M. H., Ramezania, S., and Ebrahimi, S. (2012). Potentiometric determination of nanomolar concentration of Cu(II)using a carbon paste electrode modified by a self–assembled mercapto com-pound on gold nanoparticles. Sensors and Actuators B 169: 305–311.
Park, J. S., Jeong, S., Dho, S., Lee, M., and Song, C. (2010). Colorimetric sensing of Cu2+using a cyclodextrinedyerotaxane. Dyes and Pigments 87: 49–54.
Reddy, T. S., and Reddy, A. R. (2014). 2–Hexylaminoethylamidonaphthalimide as Cu2+ sensor. SpectrochimicaActa Part A: Molecular and Biomolecular Spectroscopy 128: 880–886.
Shaltout, A. A., Boman, J., Welz, B., Castilho, I. N. B., AlAshkar, E. A., and Gaita, S. M. (2014). Method development for the determination of Cd, Cu, Ni and Pb in PM2.5 particles sampled in industrial and urban areas of Greater Cairo, Egypt, using high–resolution continuum source graphite furnace atomic absorption spectrometry. Micro chemical Journal 113: 4–9.
Supsana, P., Tsoungas, P.G., Aubry, A., Skou-lika, S., and Varvounis G. (2001). Oxidation of 1–acyl–2–naphthol oximes: peri– and o–cyclisation and spiro cyclodimerisation of naphthoquinone nitrosomethide intermediates. Tetrahedron 57: 3445–3453.
Wang, M., Leung, K. –H., Lin, S., Chan, D.S-H., Kwong, D. W. J., Leung, C. –H., and Ma, D–L. (2014). A colorimetric chemosensor for Cu2+ ion detection based on an iridium(III)complex. Scientific Report 4: 6794.
Xiang, Y., Li, Z., Chen, X., and Tong, A. (2008). Highly sensitive and selective optical chemo-sensor for determination of Cu2+ in aqueous solution. Talanta 74: 1148–1153.
Xu, Z., Pan, J., Spring, D.R., Cui, J., and Yoon, J. (2010). Ratiometric fluorescent and colorimetric sensors for Cu2+ based on 4,5–disubstituted–1,8–naphthalimide and sensing cyanide via Cu2+ displacement approach. Tetrahedron 66: 1678–1683.
Xue, X., Fang, H., Chen, H., Zhang, C., Zhu, C., Bai, Y., He, W., and Guo, Z. (2016). In vivo fluorescence imaging for Cu2+in live mice by a new NIR fluorescent sensor. Dyes and Pigments 130: 116–121.