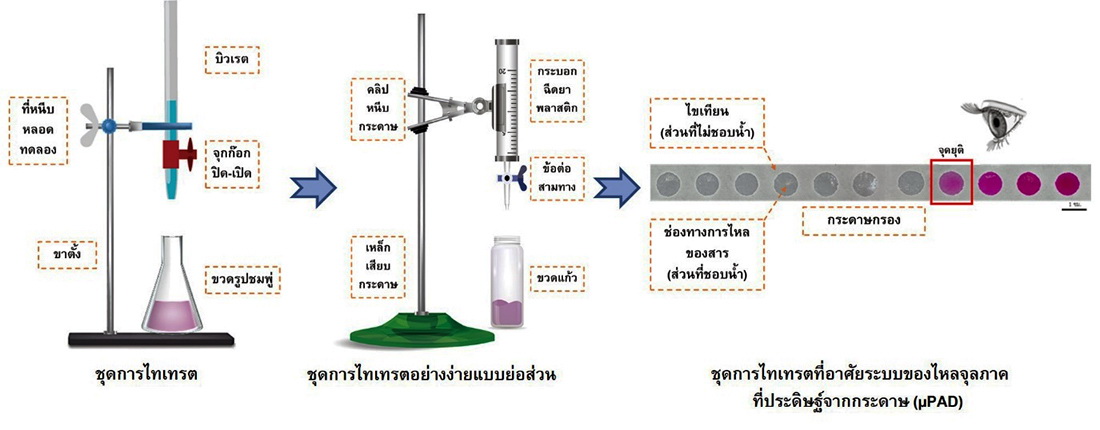
การสาธิตชุดการทดลองในวิชาเคมีที่อาศัยระบบของไหลจุลภาคที่ประดิษฐ์จากกระดาษ (µPAD) ที่สร้างโดยใช้ไขเทียนเป็นวัสดุไม่ชอบน้ำ
Main Article Content
Abstract
Phattaravan Supalert, Rattapol Meelapsom, Saksri Supasorn and Purim Jarujamrus
รับบทความ: 4 กุมภาพันธ์ 2563; แก้ไขบทความ: 21 พฤษภาคม 2563; ยอมรับตีพิมพ์: 24 พฤษภาคม 2563
บทคัดย่อ
การเรียนวิทยาศาสตร์ให้เข้าใจโดยไม่ทำปฏิบัติการโดยเฉพาะวิชาเคมีเป็นปัญหาใหญ่เรื่องหนึ่งของการศึกษาไทย ซึ่งส่วนหนึ่งมีผลมาจากจากอุปกรณ์และสารเคมีส่วนใหญ่มีราคาสูง ดังนั้นครูผู้สอนหรือนักวิจัยหลายท่านจึงพยายามพัฒนาเครื่องมือและอุปกรณ์ที่ใช้ในการทำการทดลองให้สอดคล้องกับบริบททางการศึกษาของหลายโรงเรียนที่อยู่ในเขตชนบทของประเทศไทย บทความวิจัยนี้ขอยกตัวอย่างบทปฏิบัติการ เรื่อง การไทเทรตกรด–เบส โดยทั่วไปการทำปฏิบัติการทดลองในชั้นเรียนใช้วิธีมาตรฐานที่ต้องใช้ชุดอุปกรณ์เครื่องแก้วที่มีขนาดใหญ่จำนวนมากและใช้สารเคมีปริมาณมาก จึงทำให้วิธีมาตรฐานนี้มีค่าใช้จ่ายสูง นักวิจัยจึงพัฒนาการทดลองแบบวิธีย่อส่วนเพื่อแก้ไขปัญหาดังกล่าว โดยเริ่มจากการสร้างชุดทดลองการไทเทรตอย่างง่ายแบบย่อส่วนและต้นทุนต่ำ จากนั้นพัฒนาเป็นระบบที่มีขนาดเล็กลงถึงระดับไมครอนโดยอาศัยระบบของไหลจุลภาคที่ประดิษฐ์จากกระดาษ (µPAD) ซึ่งสามารถอธิบายทฤษฎีที่เกี่ยวข้องได้เช่นเดียวกับวิธีมาตรฐาน แต่ยังมีการนำ µPAD มาประยุกต์ใช้ในด้านการศึกษาค่อนข้างน้อย ดังนั้นการนำชุดทดลองสาธิตที่อาศัย µPAD มาช่วยในการจัดการเรียนรู้จึงเป็นทางเลือกที่น่าสนใจ เนื่องจากมีข้อดีหลายประการ เช่น หาง่าย ราคาถูก ใช้สารเคมีน้อยในระดับไมโครลิตร ใช้งานง่ายโดยไม่ต้องใช้ผู้ชำนาญในการใช้เครื่องมือ พกพาสะดวก นำไปสู่แนวคิดการเป็น “เคมีสีเขียว” บทความวิจัยนี้เน้นการนำเสนอและอภิปรายการสร้างชุดการทดลองสาธิตในวิชาเคมีที่อาศัย µPAD ที่สร้างโดยใช้ไขเทียนซึ่งเป็นวัสดุไม่ชอบน้ำ โดยจะนำเสนอวิธีการสร้าง 4 วิธีที่แตกต่างกันคือ การวาดด้วยไขเทียน การพิมพ์สกรีนด้วยไขเทียน การพิมพ์ด้วยไขเทียน และการจุ่มไขเทียน
คำสำคัญ: ระบบของไหลจุลภาคที่ประดิษฐ์จากกระดาษ ไขเทียน วัสดุไม่ชอบน้ำ ชุดการทดลองในวิชาเคมี
Abstract
Learning science for understanding without laboratory work, especially chemistry, is one of the major educational problems encountered in Thailand. Lack of equipment and chemical substance are the major problems for the establishment of a laboratory course. Therefore, many teachers or researchers have been trying to develop simple tools that are suitable for the educational context where sophisticated instruments in many schools located in urban areas of Thailand are limited to access. In this article, how to miniaturize acid–base titration in the laboratory will be demonstrated and discussed. In general classrooms, conventional titration is used. This method requires a lot of glassware, high chemical volume, leading to a high cost of operation. To overcome these problems, small scale titration has been proposed which can provide simple, low–cost setup. Moreover, microfluidic paper–based analytical device (µPAD) has been further developed as a miniaturized system for acid–base titration. Besides, the use of µPAD is still challenging in an educational application, especially being an experimental kit in chemistry. Hence, demonstration of experimental kit based on µPAD can provide many advantages such as simple, low–cost, low chemical volume (microliter), easy to use, and portable which meets the concept of “Green chemistry”. Demonstration of experimental kit based on µPAD fabricated by using wax as hydrophobic material with various methods including wax drawing, wax screen printing, wax printing, and wax dipping will be proposed and discussed.
Keywords: Microfluidic paper–based analytical device (µPAD), Wax, Hydrophobic material, Experimental kit in chemistry
Downloads
Article Details

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
References
Abe, K., Suzuki, K., and Citterio, D. (2008). Inkjet–printed microfluidic multianalyte chemical sensing paper. Analytical Chemistry 80(18): 6928–6934.
Barmby, P., Kind, P. M., and Jones, K. (2008). Examining changing attitudes in secondary school science. International Journal of Science Education 30(8): 1075–1093.
Birch, N. C., and Stickle, D. F. (2003). Example of use of a desktop scanner for data acquisition in a colorimetric assay. Clinica Chimica Acta 333(1): 95–96.
Bruzewicz, D. A., Reches, M., and Whitesides, G. M. (2008). Low–cost printing of poly(dimethylsiloxane) barriers to define microchannels in paper. Analytical Chemistry 80(9): 3387–3392.
Cai, L., Wu, Y., Xu, C., and Chen, Z. (2013). A simple paper–based microfluidic device for the determination of the total amino acid content in a tea leaf extract. Journal of Chemical Education 90(2): 232–234.
Cai, L., Wang, Y., Wu, Y., Xu, C., Zhong, M., Laia, H., and Huang, J. (2014). Fabrication of a microfluidic paper–based analytical device by silanization of filter cellulose us-ing a paper mask for glucose assay. Analyst 139: 4593–4598.
Carrilho, E., Martinez, A. W., and Whitesides, G. M. (2009). Understanding wax printing: A simple micropatterning process for paper–based microfluidics. Analytical Chemistry 81(16): 7091–7095.
Chatmontree, A., Chairam, S., Supasorn, S., Amatatongchai, M., Jarujamrus, P., Tamuang, S., and Somsook, E. (2015). Student fabrication and use of simple, low–cost, paper–based galvanic cells to investigate electrochemistry. Journal of Chemical Education 92(6): 1044–1048.
Chen, B., Kwong, P., and Gupta, M. (2013). Patterned fluoropolymer barriers for containment of organic solvents within paper–based microfluidic devices. ACS Applied Materials & Interfaces 5(23): 12701–12707.
Dean, J. A. (1999). Lange’s Handbook of Chemistry. 15th ed. Chicago, Illinois: R. R. Donnelley & Sons.
Din–a, A., Tamuang, S., Amatatongchai, M., Jarujamrus, P., and Chairam, S. (2016). Simple, low–cost and small scale titration set for microscale laboratory in classroom. Journal of Research Unit on Science, Technology and Environment for Learning 7(2): 424–436.
Dornelas, K. L., Dossi, N., and Piccin, E. (2015). A simple method for patterning poly(dimethylsiloxane) barriers in paper using con-tact–printing with low–cost rubber stamps. Analytica Chimica Acta 858(1): 82–90.
Dungchai, W., Chailapakul, O., and Henry, C. S. (2011). A low–cost, simple, and rapid fabrication method for paper–based micro fluidics using wax screen–printing. Analyst 136(1): 77–82.
Fenton, E. M., Mascarenas, M. R., López, G. P., and Sibbett, S. S. (2009). Multiplex la-teral–flow test strips fabricated by two–dimensional shaping. ACS Applied Ma-terials & Interfaces 1(1): 124–129.
George, R. (2000). Measuring Change in Students’ attitudes toward science over time: An application of latent variable growth modeling. Journal of Science Education and Technology 9(3): 213–225.
He, Q., Ma, C., Hu, X., and Chen, H. (2013). Method for fabrication of paper–based microfluidic devices by alkylsilane self–assembling and UV/O3–patterning. Analytical Chemistry 85(3): 1327–1331.
Karita, S., and Kaneta, T. (2014). Acid–base titrations using microfluidic paper–based analytical device. Analytical Chemistry 86(24): 12108–12114.
Koesdjojo, M. T., Pengpumkiat, S., Wu, Y., Boonloed, A., Huynh, D., Remcho, T. P., and Remcho, V. T. (2015). Cost effective paper–based colorimetric microfluidic devices and mobile phone camera readers for the classroom. Journal of Chemical Education 92(4): 737–741.
Lai, H., Li, Z., Zhu, S., Cai, L., Xu, C., and Zhou, Q. (2020). Naked–eye detection of aluminum in gastric drugs on a paper based analytical device. Journal of Chemical Education 97(1): 295–299.
Lertsuwunpaisal, P., Yoome, P., and Srisopa, A. (2016). Titration technique development based on microscale and the implement in science classes. Humanities and Social Sciences Journal of Graduate School, Pibulsongkram Rajabhat University 10(2): 18–36.
Li, X., Tian, J., Nguyen, T., and Shen, W. (2008). Paper–based microfluidic devices by plasma treatment. Analytical Chemistry 80(23): 9131–9134.
Li, X., Tian, J., Garnier, G., and Shen, W. (2010). Fabrication of paper–based microfluidic sensors by printing. Colloids and Surfaces B: Biointerfaces 76: 564–570.
Mako, T. L., and Levine, M. (2019). Design, implementation, and evaluation of paper-based devices for the detection of acetaminophen and phenacetin in an advanced undergraduate laboratory. Journal of Chemical Education 96(8): 1719–1726.
Martinez, A. W., Phillips, S. T., Butte, M. J., and Whitesides, G. M. (2007). Patterned paper as a platform for inexpensive, low–volume, portable bioassays. Angewandte Chemie International Edition 46(8): 1318–1320.
Namwong, P., Jarujamrus, P., Amatatong-chai, M., and Chairam, S. (2018). Fabricating simple wax screen–printing paper-based analytical devices to demonstrate the concept of limiting reagent in acid–base reactions. Journal of Chemical Education 95(2): 305–309.
Nie, J., Zhang, Y., Lin, L., Zhou, C., Li, S., Zhang, L., and Li, J. (2012). Low–cost fabrication of paper–based microfluidic devices by one–step plotting. Analytical Chemistry 84(15): 6331–6335.
Nogueira, S. A., Sousa, L. R., Silva, N. K. L., Rodrigues, P. H. F., and Coltro, W. K. T. (2017). Monitoring acid–base titrations on wax printed paper microzones using a smartphone. Micromachines 8(5): 139.
Nurak, T., Praphairaksita, N., and Chailapakul, O. (2013). Fabrication of paper–based devices by lacquer spraying method for the determination of nickel (II) ion in waste water. Talanta 114: 291–296.
Olkkonen, J., Lehtinen, K., and Erho, T. (2010). Flexographically printed fluidic structures in paper. Analytical Chemistry 82(24): 10246–10250.
Patnaik, P. (2004). Dean’s Analytical Chemistry Handbook. 2nd ed. New York: McGraw–Hill.
Pena–Pereira, F. J. (2014). Miniaturization in Sample Preparation. Berlin: Walter de Gruyter GmbH.
Pimdee, N. (2020) Green Chemistry. Retreived from https://www.scimath.org/lesson-chem istry/item/7167-green-chemistry, January 14, 2020. (in Thai)
Prabpal, J., Vilaivan, T., and Praneenararat, T. (2017). Paper–based heavy metal sensors from the concise synthesis of an anionic porphyrin: A practical application of organic synthesis to environmental chemistry. Journal of Chemical Education 94(8): 1137–1142.
Pruekpramool, C., Phonphok, N., White, O. L., and Musikul, K. (2011). Student attitudes toward science: The case of Thai upper secondary school non–science students. The International Journal of Learning 18(1): 289–301.
Ravgiala, R. R., Weisburd, S., Sleeper, R., Martinez, A., Rozkiewicz, D., Whitesides, G. M., and Hollar, K. A. (2014). Using paper–based diagnostics with high school students to model forensic investigation and colorimetric analysis. Journal of Chemical Education 91(1): 107–111.
Sameenoi, Y., Nongkai, P. N., Nouanthavong, S., Henry, C. S., and Nacapricha, D. (2014). One–step polymer screen–printing for microfluidic paper–based analytical device (µPAD) fabrication. Analyst 139: 6580–6588.
Sharpe, E., and Andreescu, S. (2015). Integration of nanoparticle–based paper sen-sors into the classroom: An example of application for rapid colorimetric analysis of antioxidants. Journal of Chemical Education 92(5): 886–891.
Smith, S., Moodley, K., Govender, U., Chen, H., Fourie, L., Ngwenya, S., Kumar, S., Mjwana, P., Cele, H., Mbanjwa, M. B., Potgieter, S., Joubert, T. H., Land, K. (2015). Paper–based smart microfluidics for education and low–cost diagnostics. South African Journal of Science 111: 1–10.
Songjaroen, T., Dungchai, W., Chailapakul, O., and Laiwattanapaisal, W. (2011). Novel, simple and low–cost alternative method for fabrication of paper–based microfluidics by wax dipping. Talanta 85(5): 2587–2593.
Taghizadeh–Behbahani, M., Hemmateenejad, B., and Shamsipur, M. (2018). Colorimetric determination of acidity constant using a paper–based microfuidic analytical device. Chemical Papers 72(5): 1239–1247.
Wang, B., Lin, Z., and Wang, M. (2015). Fabrication of a paper–based microfluidic device to readily determine nitrite ion con-centration by simple colorimetric assay. Journal of Chemical Education 92(4): 733–736.
Xu, C., Lin, W., and Cai, L. (2016). Demonstrating electrophoretic separation in a straight paper channel delimited by a hydrophobic wax barrier. Journal of Chemical Education 93(5): 903–905.